在mRNA疫苗、基因编辑和核酸治疗快速发展的背景下,脂质纳米颗粒(LNP)仍是核心递送平台。随着行业技术的持续进步,LNP配方与工艺设计进入了精细化与功能化的新阶段。中新康明紧跟这一趋势,全面升级其核酸-LNP制剂CDMO服务能力,为客户提供更多战略弹性与技术深度。
聚焦行业前沿:LNP技术的新趋势
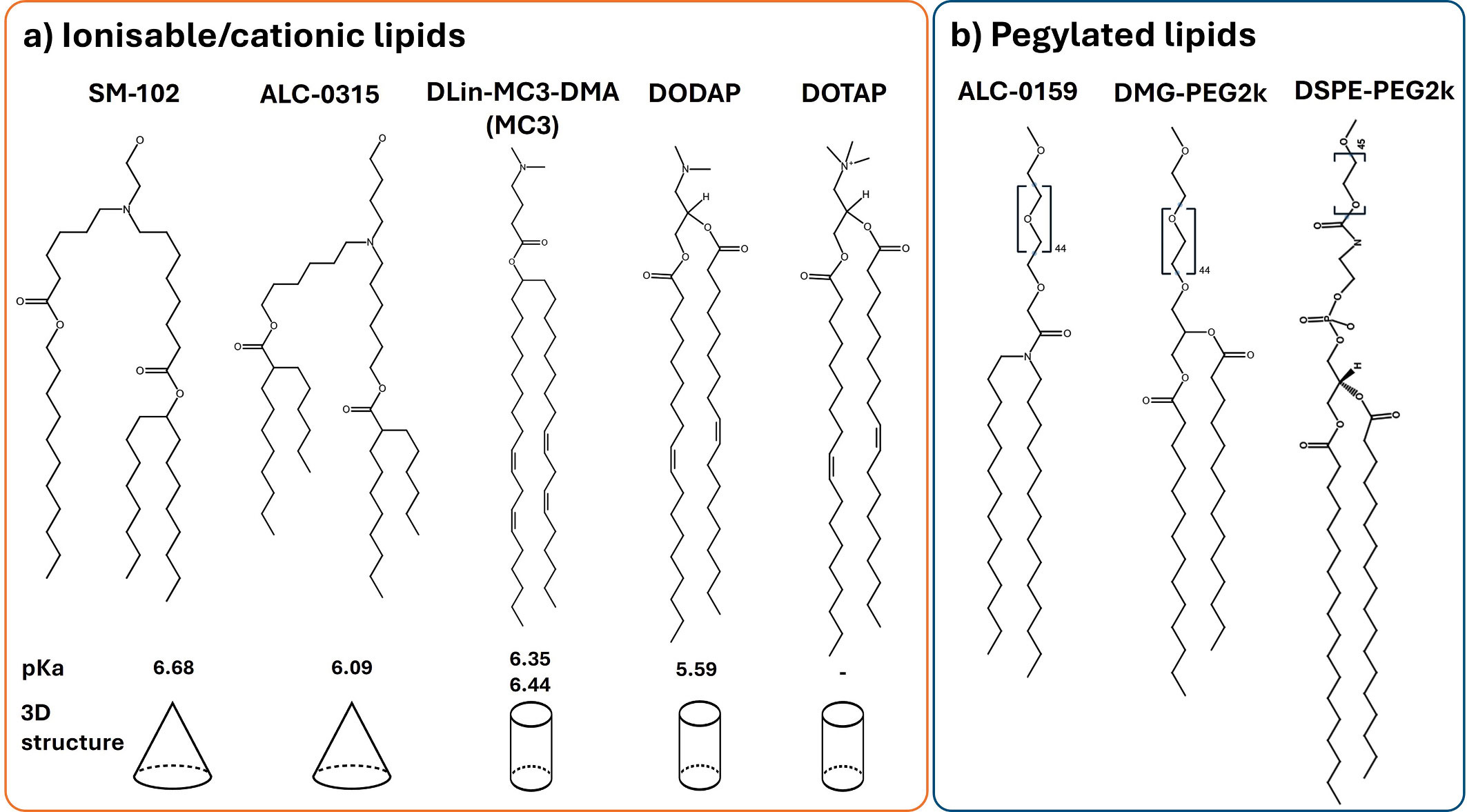
离子化脂质PK/BD差异机制:最近一项研究系统比较了SM-102、ALC-0315和MC3等离子化脂质对mRNA-LNP的体内药代动力学(PK)与生物分布(BD)的影响。研究发现,不同脂质虽然其理化性质(粒径、封装效率等)相似,但在mRNA血浆保护、循环时间和表达分布方面存在显著差异。特别是SM-102展现出极佳的mRNA保护能力,而ALC-0315虽然延长脂质循环寿命,却降低mRNA的体内滞留。
中新康明LNP-CDMO服务能力优化与战略升级
基于以上行业趋势和科学前沿,中新康明进一步加强和拓展其LNP-CDMO服务能力,以更好服务于mRNA和核酸药物领域的创新客户。以下是优化后的服务内容与优势。
1.核酸-LNP配方设计与精细优化
电离脂质筛选与深度对比:凭借对SM-102、ALC-0315、MC3等领域领先脂质的系统理解,我们能帮助客户依据PK/BD特性(如循环时间、mRNA保护、组织分布)选择合适的脂质组合。
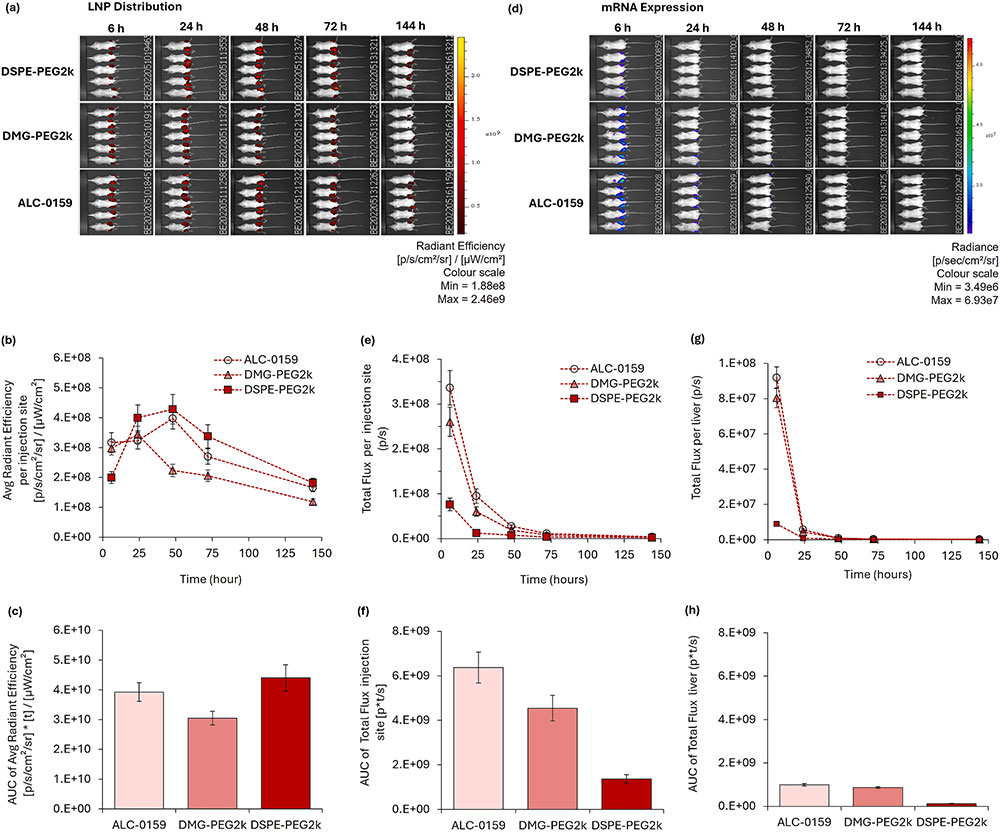
PEG脂质设计与动力学调控:结合最新研究(例如DMG-PEGvsDSG-PEG),我们的团队支持客户在PEG链长和解离速度上进行策略性优化,以适配不同给药途径(IV/SC/IM)和治疗应用。
结构-功能关联模型:通过与客户共同建立体外(细胞)、体内(小鼠)评价体系,并整合形态学(FRET/SAXS/EM)数据,中新康明能够桥接理化属性与体内效力之间的差异,为配方提供科学指导。
2.工艺开发与缓冲体系工程
先进微流控制备:我们继续采用微流控、乙醇注射等技术,同时综合行业对pH重构机制的认识,优化缓冲液切换策略,从而实现稳定LNP制剂的生产。
pH转换优化:依据最新关于形态重构(重构阶段、融合行为)的研究,我们设计缓冲转移流程(如酸性环境到中性环境)时最大限度减少颗粒破坏或融合,以提高稳定性和表达性能。
可扩展、可复制的工艺参数优化:我们在流速比(FRR)、总流量比(TFR)、离子强度、pH等关键变量上积累经验,确保生产的可重复性和批间一致性。
3.中试与放大:为临床和商业化提供强大产能
完善的GMP中试车间支持从克级到公斤级生产。
连续流动合成平台与淋注/灌装能力保证制剂质量和生产效率。
在线监控(如粒径、Zeta电位、过程参数)和质量追踪系统确保工艺稳定性与可追溯性。
4.分析表征与质量控制
物理特性测定:包括粒径(DLS)、PDI、多种pH条件下结构分析(SAXS/FRET/EM)等。
化学组成与封装分析:定量脂质组成(LC-MS)、残留溶剂、缓冲体系成分分析。
核酸完整性与效力检测:mRNA含量、完整性(电泳、QPCR)、稳定性研究(加速和长期)、释放性能。
转染和表达功能性测试:体外细胞转染(例如HEK293或HeLa)、体内报告基因(动物模型)等。
方法开发与方法验证:符合监管(CMC)要求,支持IND/CTA申报文件。
5.临床及商业化支持
技术转移与工艺验证:从研发到GMP批次建立标准化转移流程。
CMC/QA文件撰写:我们协助编写工艺说明书、批记录、质量规格、稳定性报告等。
监管申报支持:结合最新科学研究(如PK/BD数据、结构行为研究)提供科学论据,为监管机构提供强有力的CMC支持。
商业化规模生产:确保持续、可扩展供应,同时协调生产和质量体系,以适应客户全球化推进需求。
参考文献:“Exploring the impact of commonly used ionizable and pegylated lipids on mRNA-LNPs: A combined in vitro and preclinical perspective”
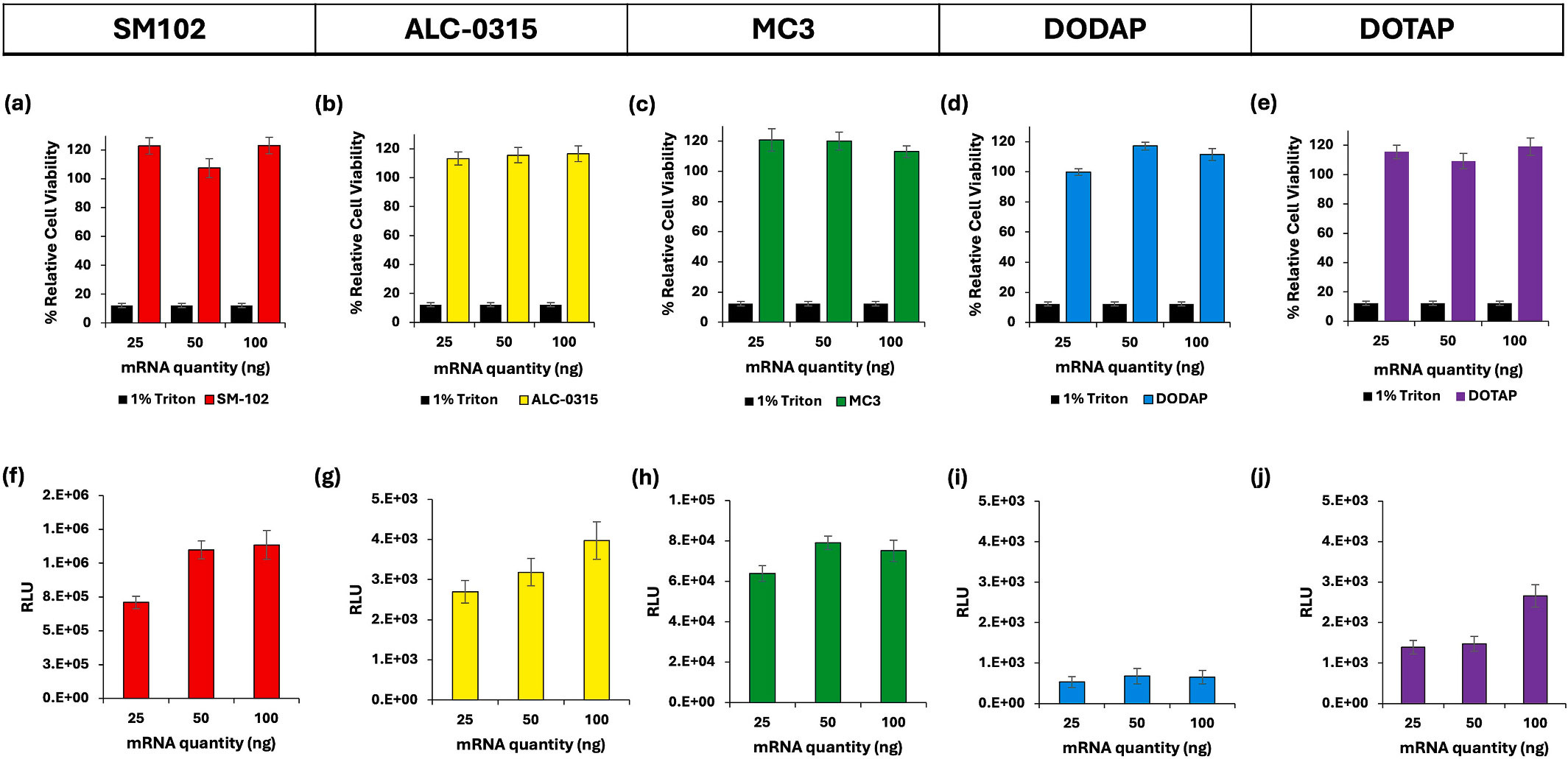
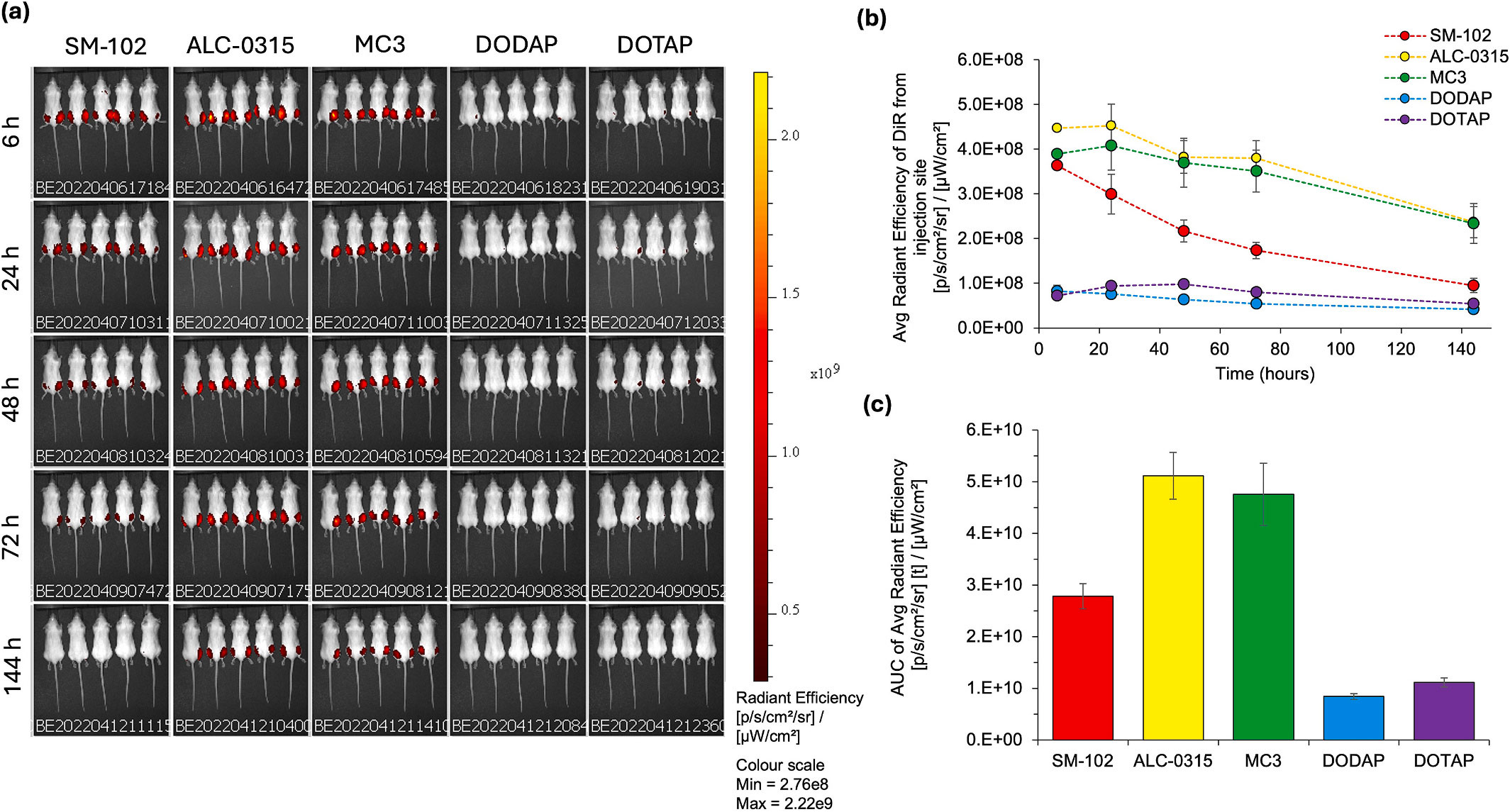
文献摘要:可电离脂质被公认为脂质纳米颗粒(LNPs)的关键成分。它们能够封装 mRNA,保护其免受酶降解,促进细胞摄取,并促进其在细胞质中的释放,以便后续翻译成蛋白质。此外,聚乙二醇化脂质被添加以稳定颗粒在储存和体内的状态。在本研究中,我们使用常见的可电离和聚乙二醇化脂质制备 LNPs,并在体外(使用 HEK293 细胞)和体内(小鼠研究)评估其效力,以考虑结构对效力的影响。所有 LNPs 配方均采用固定摩尔比的 DSPC:胆固醇:可电离/阳离子脂质:聚乙二醇脂质(10:38.5:50:1.5 摩尔%)制备。所有 LNP 配方均表现出相似的关键质量属性(CQAs),包括粒径<100 纳米,低多分散指数(<0.2),接近中性的 Zeta 电位,以及高封装效率(>90%)。然而,这些 LNPs 的效力,通过体外 mRNA 表达和小鼠肌肉注射后的体内表达来衡量,差异显著。使用 SM-102 配方的 LNPs 表现出最高的效力。在体外实验中,而体内实验表明,SM-102 和 ALC-0315 脂质纳米颗粒(LNP)的 mRNA 表达显著高于 DLin-MC3-DMA(MC3)、DODAP 和 DOTAP 脂质纳米颗粒。我们还研究了聚乙二醇脂质的选择(ALC-0159、DMG-PEG2k 和 DSPE-PEG2k)的影响,这并未对脂质纳米颗粒的关键质量属性(CQAs)以及它们从注射部位的清除产生影响。然而,聚乙二醇脂质的选择显著影响了 mRNA 的表达,加入 DSPE-PEG2k 会降低表达。这项工作为不断发展的 mRNA 研究领域提供了宝贵的见解,强调关键质量属性是脂质纳米颗粒生产过程质量的标志,但不能区分脂质纳米颗粒的效力。同样,标准的体外研究也无法提供体内效力的见解。这些结果进一步强调了配方设计的复杂性以及弥合不同实验环境之间差距的重要性。
中新康明在LNP-CDMO领域的差异化竞争优势
前沿科学驱动:我们紧跟行业最新研究(如离子化脂质PK/BD、PEG动力学、形态重构机制),将这些前沿科学成果内化为服务能力。
定制化与灵活性:针对不同给药途径(SC、IV、IM)、治疗应用(疫苗、基因编辑、蛋白替代)等场景,我们可提供高度定制的配方和工艺设计。
端到端一站式服务能力:涵盖配方设计、工艺开发、中试/放大、分析表征、临床注册支持及长期商业生产。
高质量与监管准备:具备严格GMP管理、全面分析平台与CMC文档经验,帮助客户顺利通过IND/CTA审评。
技术创新与前瞻视野:我们不仅满足当前主流LNP(如SM-102/ALC-0315)的生产需求,还致力于支持新型脂质(如FS01)开发,为下一代mRNA递送载体助力。
总结
在LNP技术快速演进的当下,新一代mRNA和核酸药物的成功越来越依赖于精细化、机制驱动的制剂设计与开发策略。中新康明凭借深厚技术积累、持续创新的服务能力,以及对行业前沿趋势(如脂质结构-功能关系、PEG动力学、形态重构机制)的深刻理解,为客户提供真正差异化、高价值的LNPCDMO解决方案。我们致力于与全球创新药企携手,共同加速mRNA和核酸疗法的临床转化与高效商业化落地。
 返回
返回