在全球癌症治疗不断向精准化、个性化方向迈进的趋势下,实体肿瘤由于其高度异质性、复杂的微环境以及基因突变的多样性,仍然是药物研发领域最具挑战性的方向之一。近年来,CRISPR/Cas9技术以其强大的基因编辑能力,为纠正致癌基因、沉默驱动突变和修复损伤通路提供了前所未有的可能。然而,如何将CRISPR系统高效、安全地递送至肿瘤细胞,仍然是从实验室迈向临床的最大瓶颈。
最新的研究进展显示,脂质纳米颗粒(LNPs)正在成为突破该瓶颈的核心技术。作为一种具有良好生物相容性、可工程化的核酸递送平台,LNP能够高效封装Cas9mRNA、sgRNA或RNP复合物,保护其免受体内降解,并使其精准到达肿瘤组织,从而显著增强编辑效率并降低脱靶风险。多项临床前模型已表明,通过LNP递送CRISPR组件,能在肿瘤组织中实现关键致癌基因的敲除,进而抑制肿瘤生长甚至诱导肿瘤消退,为实体肿瘤提供了革命性的基因治疗路径。
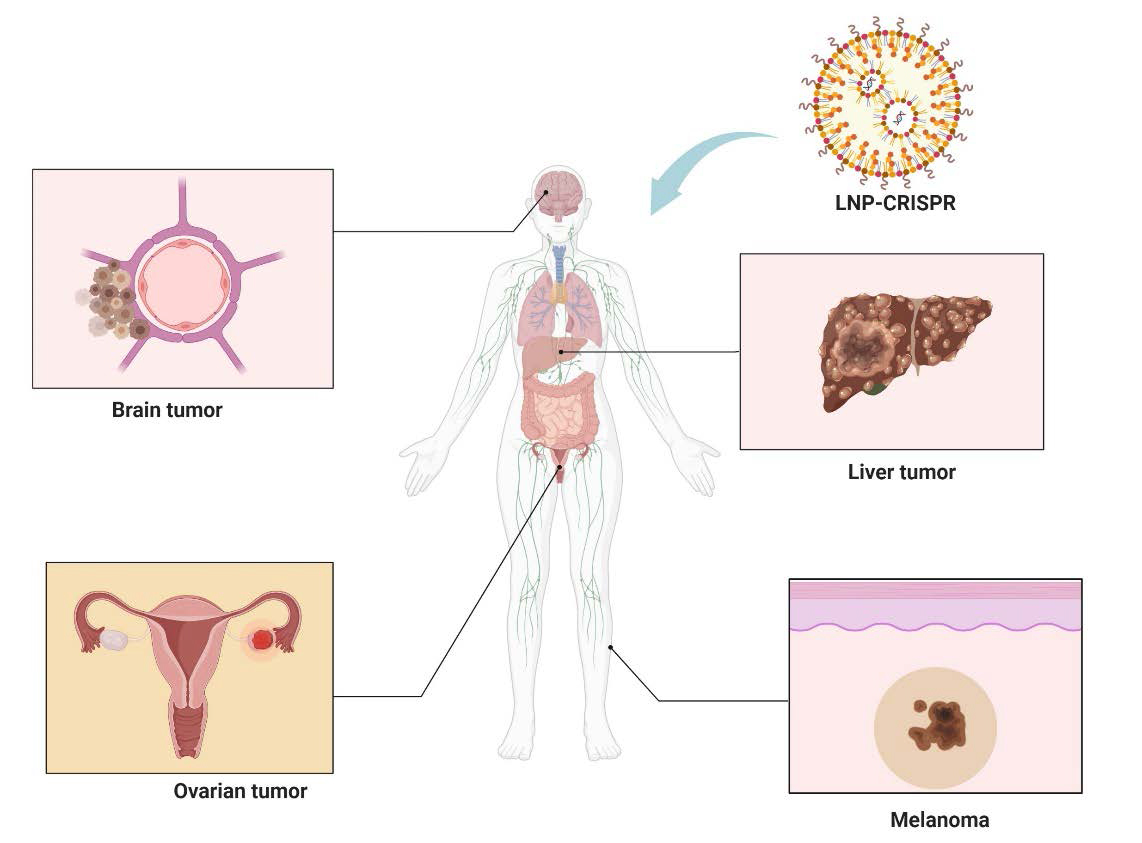
在这一趋势推动下,中新康明持续布局实体肿瘤基因编辑领域,依托完善的核酸递送平台、脂质原料供应体系与制剂CDMO产能,为行业提供从材料、工艺、开发到生产的一体化解决方案,加速CRISPR基因治疗从科研走向临床转化。
实体肿瘤治疗的未来:从化疗到基因编辑的代际飞跃
实体瘤治疗长期依赖手术、放疗和化疗,但这些传统方式往往受到耐药性、毒副作用以及肿瘤异质性的限制。CRISPR/Cas9的出现,为精准定位致癌基因及关键通路提供了工具,使“从根本纠正肿瘤驱动力”成为可能。
然而,CRISPR组件体积大、结构复杂、对体内环境高度敏感,直接给药几乎无法实现有效编辑。因此,载体技术成为CRISPR疗法能否真正临床化的最关键因素。
与病毒载体相比,LNP技术具有以下临床级优势:
可递送多类CRISPR组件(Cas9mRNA、sgRNA、RNP)
避免病毒载体引发的长期整合风险
可调控的尺寸、组分、表面特性,使其更易穿透肿瘤组织
良好的免疫安全性,便于多次给药
可进行工业化放大、与mRNA工艺兼容
随着多项研究验证LNP-CRISPR在肿瘤模型中的显著抑瘤效果,行业已将“LNP作为基因编辑药物的核心递送系统”视为明确趋势。

中新康明提供CRISPR基因治疗所需的LNP原料体系与CDMO一体化服务
面向实体肿瘤治疗的特殊需求,中新康明建立了覆盖原料生产到制剂工艺开发的全流程平台,包括:
1.CRISPR递送专用LNP原料产品
公司可稳定供应多类适用于CRISPR的脂质原料,包括:
高效可电离脂质(MC3、LC系列、专为RNP递送开发的阳离子脂质)
DSPC、胆固醇等结构脂质
PEG脂质及改性PEG替代物
适用于肿瘤靶向的新型脂质衍生物
IND申报所需的齐全质量文件与分析方法
这些原料已被广泛应用于mRNA疫苗、siRNA药物、CRISPR基因编辑等多个研发管线。
2.CRISPR-LNP配方开发与制剂工艺CDMO服务
中新康明拥有成熟的CRISPR递送制剂开发体系,可提供:
Cas9mRNA、sgRNA、RNP的封装工艺开发
针对实体瘤的高渗透增强型LNP配方筛选
微流控工艺放大与质控体系
冻干工艺、长期稳定性研究
中试至GMP生产支持
CMC、IND申报资料撰写辅导
结合肿瘤治疗的临床需求,公司可实现粒径调控(60–120nm)、包封效率提升、渗透能力优化等多项关键工艺开发。
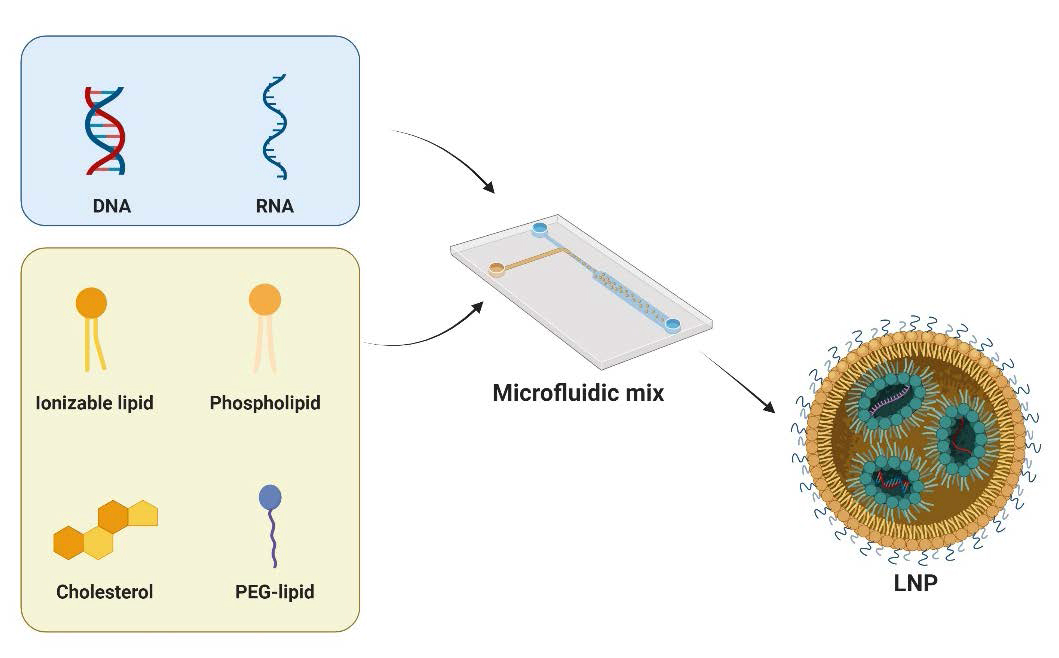
中新康明的技术优势:实现从“递送难题”到“临床可能”的跨越
中新康明在核酸递送和CRISPR工艺开发方面拥有多层核心技术:
公司建立了符合国际规范的LNP评价体系,可从粒径、Zeta电位、包封效率到细胞转染、基因敲除效率等多维度进行系统优化。同时,在体外细胞模型(乳腺癌、胰腺癌、黑色素瘤等)与动物模型中积累了大量CRISPR-LNP的递送与编辑数据,为客户提供科学决策依据。
在生产端,公司实现从mg级研发批到多百克级中试批的无缝放大能力,并可为海外IND申报提供配套质量体系(QbD、ICHM4Q等)。
通过这些体系化能力,中新康明正在成为国内少数可承接CRISPR基因治疗制剂开发的CDMO企业之一。
典型案例:LNP-CRISPR在实体瘤模型中的有效性验证
在与合作伙伴的联合项目中,中新康明开发的CRISPR-LNP系统成功在实体瘤模型中实现关键致癌基因的敲除,表现出:
明显抑制肿瘤生长
器官脱靶明显降低
优秀的Cas9mRNA翻译与sgRNA高效递送
多次给药耐受性良好
在部分模型中观察到肿瘤缩小趋势
这一案例进一步证明了LNP作为CRISPR治疗递送体系的临床可行性,也验证了中新康明在基因编辑递送工艺方面的技术实力。
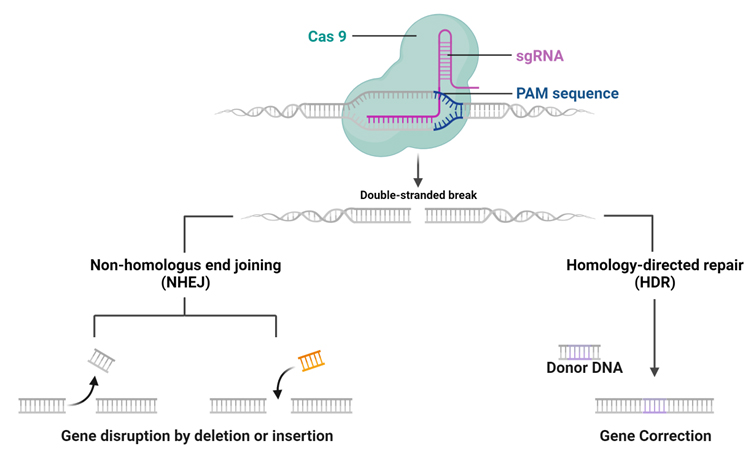
参考文献:“A landscape of recent advances in lipid nanoparticles and their translational potential for the treatment of solid tumors”
文献节选:实体肿瘤因其复杂的细胞结构和遗传异质性,长期以来一直是治疗上的难题。CRISPR基因组编辑系统的出现为精准基因干预提供了希望。然而,从实验室到临床应用的道路充满障碍,其中最大的障碍在于如何将CRISPR组分高效地递送至肿瘤细胞。脂质纳米颗粒(LNPs)已成为一种潜在的解决方案。这种生物相容性纳米材料能够封装CRISPR/Cas9系统,确保靶向递送,同时减少脱靶效应。临床前研究强调了LNP介导的CRISPR递送的有效性,显著破坏了致癌通路,并导致肿瘤消退。总体而言,CRISPR/Cas9技术与LNPs相结合,为癌症治疗提供了一种开创性的方法,具有精准、高效和解决当前局限性的潜力。尽管还需要进一步的研究和临床试验,但基于CRISPR/Cas9的个性化癌症治疗的未来充满希望。
结语:中新康明助力CRISPR基因编辑药物迈向实体肿瘤治疗的新纪元
CRISPR/Cas9技术与LNP递送体系的结合正在重塑肿瘤治疗格局,使得精准、可程序化、可定制的基因治疗不再遥远。面对这一创新浪潮,中新康明将持续投入原料创新、递送平台开发以及CDMO能力建设,为行业提供更可靠、更高效、更具临床转化价值的综合性方案。
未来,中新康明将继续携手科研机构与生物医药企业,共同推动CRISPR基因编辑治疗从临床前研究走向真正的患者获益。
 返回
返回