【摘要】
盐酸多柔比星脂质体是全球首个成功商业化的脂质体抗肿瘤药物,其问世标志着纳米药物递送技术正式走向临床。相较于游离型多柔比星,脂质体制剂在疗效、安全性及药代动力学方面均实现质的飞跃。然而,从实验室研究到产业化量产,脂质体药物仍面临处方筛选、工艺放大及质量一致性等核心挑战。
中新康明凭借深厚的脂质化学与制剂工程技术积累,为药企提供处方优化、工艺开发、中试放大及公斤级GMP生产的一体化CDMO解决方案,助力脂质体药物快速转化与产业落地,加速经典制剂的现代化升级。
一、盐酸多柔比星脂质体:经典药物的“二次新生”
多柔比星是临床应用广泛的蒽环类抗肿瘤药物,广泛用于乳腺癌、卵巢癌、多发性骨髓瘤、卡波西肉瘤等疾病。然而,其严重的心脏毒性和广泛分布限制了疗效。通过脂质体包封后,药物被精准递送至肿瘤部位,大幅降低心脏暴露量。
典型的盐酸多柔比星脂质体处方由HSPC(氢化大豆磷脂)+Cholesterol(胆固醇)+mPEG2000-DSPE(PEG修饰脂质)构成,并采用pH梯度主动装载技术实现>90%的包封率。
这种PEG修饰长循环脂质体系统可显著延长血浆半衰期(达50–70小时)、提升肿瘤靶向富集,同时降低系统性毒性,是纳米药物商业化的成功范例。
二、产业化挑战:从处方到放大的“技术鸿沟”
虽然盐酸多柔比星脂质体在临床上已取得成功,但其制备过程复杂,产业化放大面临多重技术壁垒:
处方优化复杂:脂质种类、摩尔比、相转变温度均会影响包封率与释放曲线;
工艺放大难度高:微流控、挤出、均质等关键工序对温度与剪切力极为敏感;
质量一致性要求严苛:粒径分布(80–120nm)、PDI(<0.2)、渗漏率、稳定性均为关键控制指标;
放大重现性挑战:从实验室克级到公斤级批次间需实现工艺参数等比例映射。
这些因素决定了脂质体药物从研发到商业化需要系统性的工程能力与质量体系支撑。
三、中新康明:从研发到公斤级生产的一体化CDMO平台
中新康明凭借在脂质材料、制剂工程与放大技术上的深厚积累,建立了完善的脂质体药物开发平台,能够为药企提供全流程支持。
1.处方筛选与优化
多维脂质组合筛选体系(HSPC、DSPC、DSPE-PEG、Cholesterol等);
高通量筛选确定最优脂质摩尔比与装载参数;
优化pH梯度装载工艺,实现高包封率与稳定性。
2.工艺开发与质量控制
采用微流控+高压均质技术,控制粒径均一(80–120nm);
建立QbD(质量源于设计)体系,实现参数与性能的线性映射;
完善的分析方法体系,包括粒径、PDI、包封率、渗漏率、释放曲线等关键指标。
3.中试放大与公斤级GMP生产
拥有10L–100L连续脂质体生产线;
GMP级洁净区满足药用脂质与制剂生产规范;
实现公斤级中间体及原液生产,支持IND及注册批次制备。
4.CDMO与注册支持服务
提供从研发批到注册批的技术转移与工艺验证;
协助客户完成中、美、欧法规文件与IND申报资料撰写;
提供稳定性研究与一致性验证服务。
四、未来展望:从经典药物到智能递送系统
在盐酸多柔比星脂质体成功商业化的基础上,脂质体技术正迈向更高层次的创新:
多药协同载体系统(如多柔比星+紫杉醇/siRNA);
环境响应型脂质体(pH/酶/温敏释放系统);
靶向修饰递送系统(表面偶联抗体或配体);
核酸与小分子融合平台(融合mRNA/siRNA与化疗药物)。
中新康明正在拓展脂质体与RNA药物递送平台的融合开发,构建从小分子到大分子药物的统一纳米递送体系。
五、引用文献
“Tangeretin-Assisted Platinum Nanoparticles Enhance the Apoptotic Properties of Doxorubicin: Combination Therapy for Osteosarcoma Treatment”
Nanomaterials 2019, 9(8), 1089; https://doi.org/10.3390/nano9081089
点击查看文献源文件:

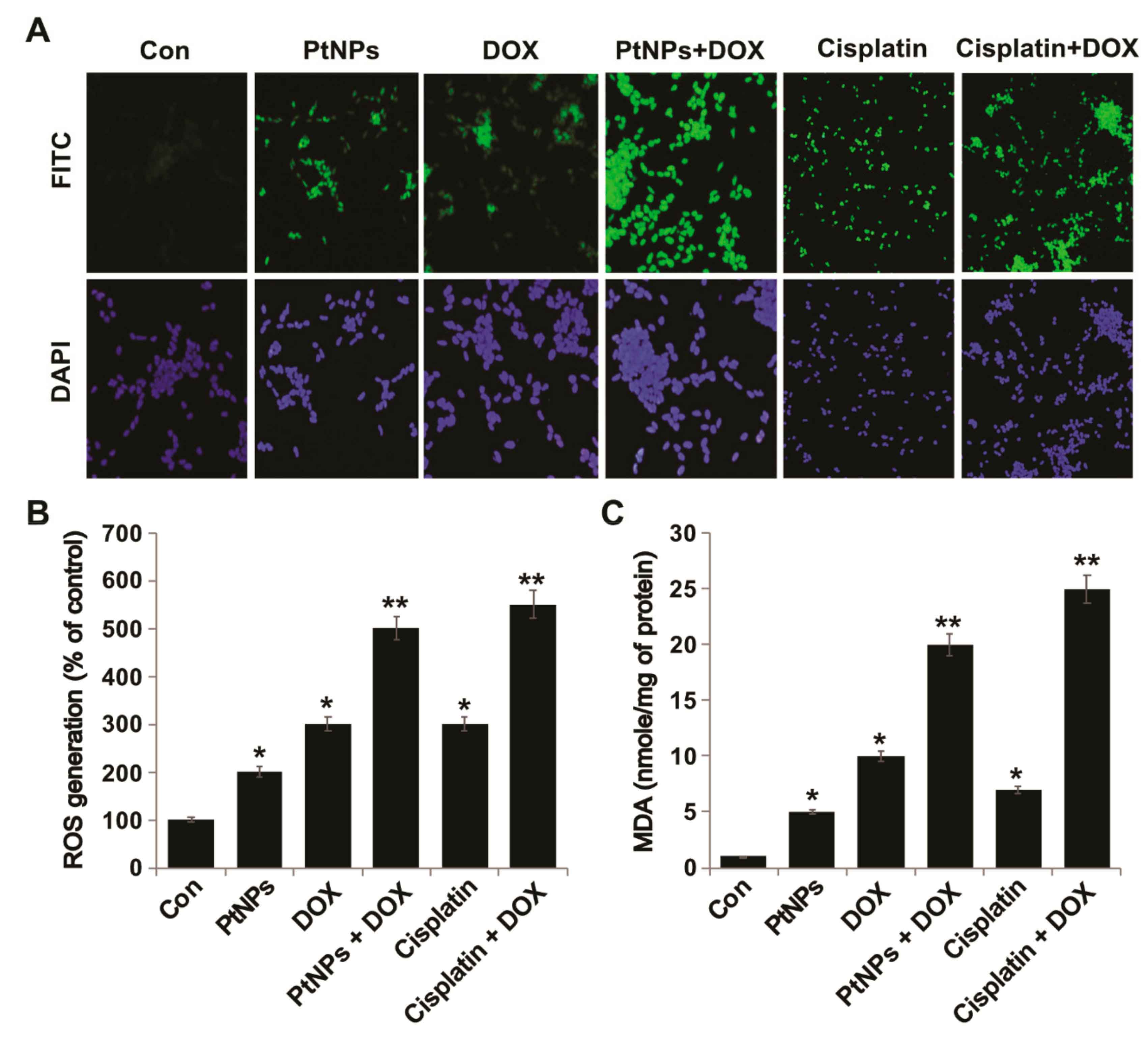
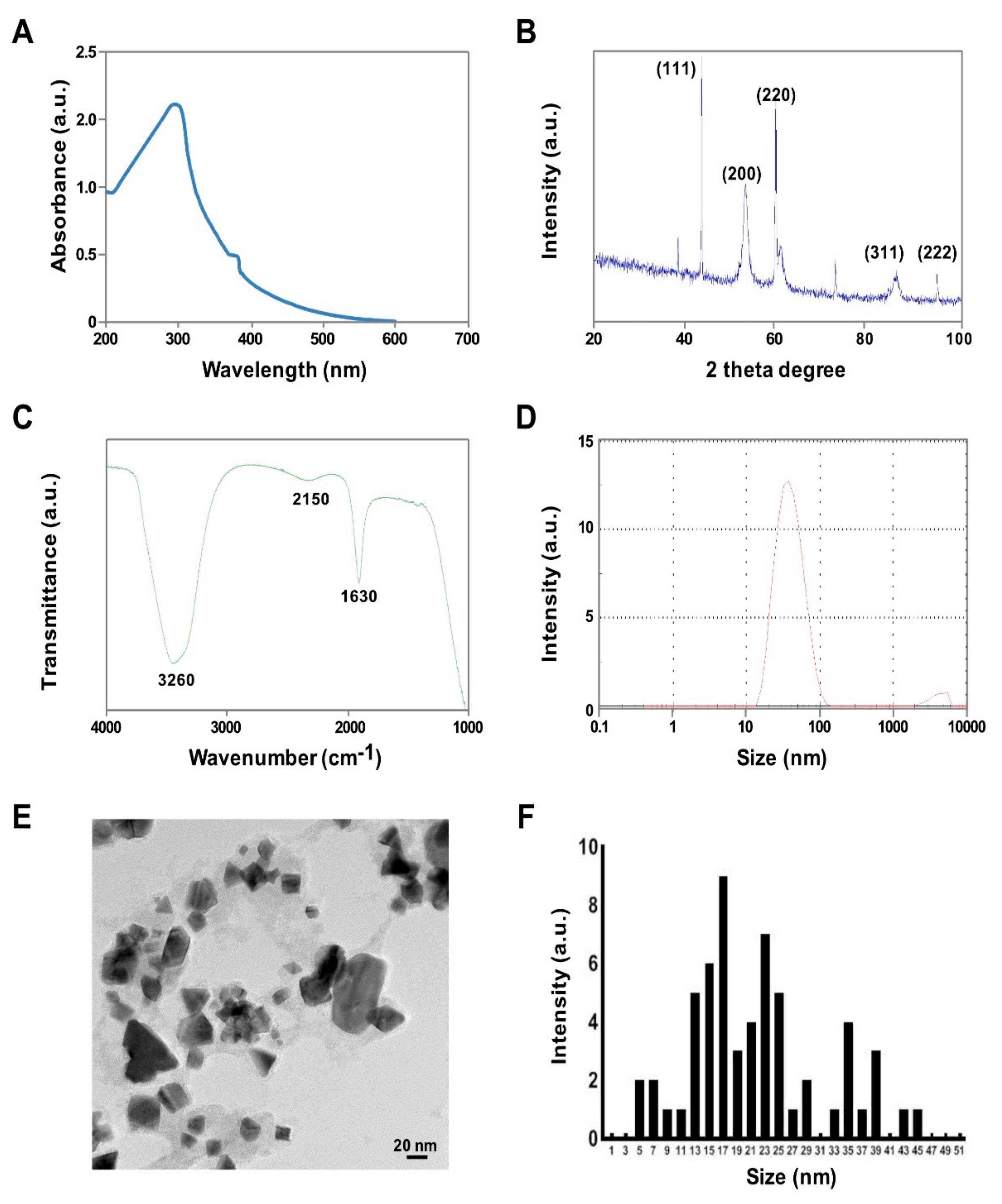
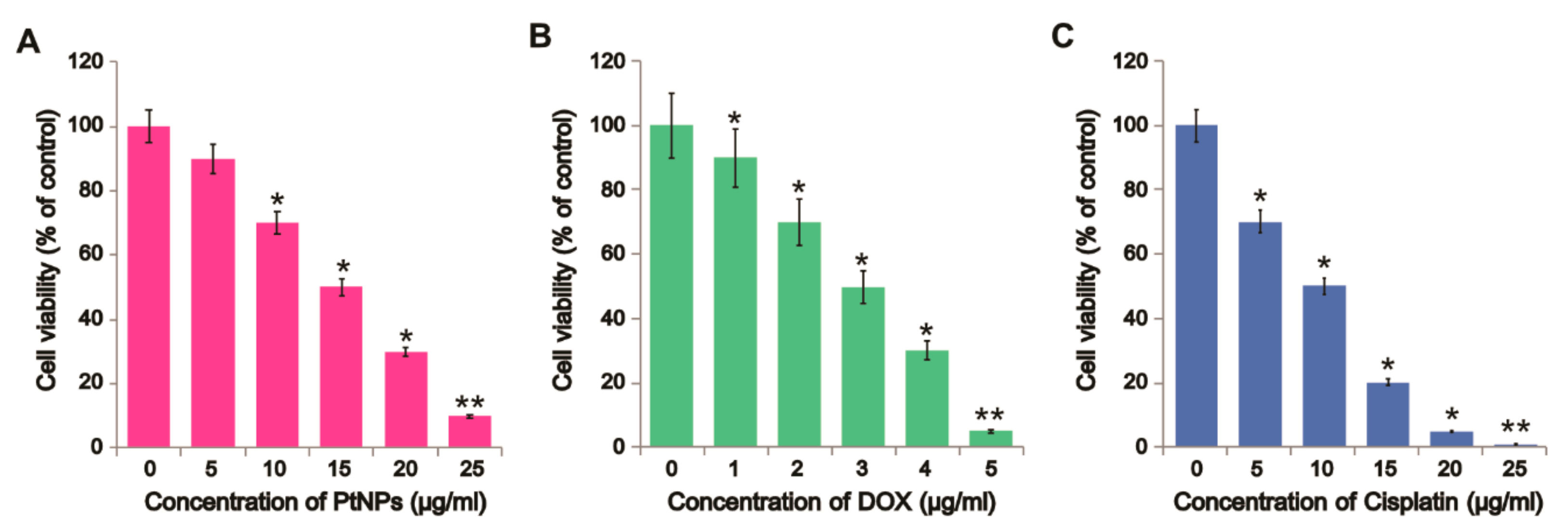
节选:Osteosarcoma (OS) is the most common type of cancer and the most frequent malignant bone tumor in childhood and adolescence. Nanomedicine has become an indispensable field in biomedical and clinical research, with nanoparticles (NPs) promising to increase the therapeutic efficacy of anticancer drugs. Doxorubicin (DOX) is a commonly used chemotherapeutic drug against OS; however, it causes severe side effects that restrict its clinical applications. Here, we investigated whether combining platinum NPs (PtNPs) and DOX could increase their anticancer activity in human bone OS epithelial cells (U2OS). PtNPs with nontoxic, effective, thermally stable, and thermoplasmonic properties were synthesized and characterized using tangeretin. We examined the combined effects of PtNPs and DOX on cell viability, proliferation, and morphology, reactive oxygen species (ROS) generation, lipid peroxidation, nitric oxide, protein carbonyl content, antioxidants, mitochondrial membrane potential (MMP), adenosine tri phosphate (ATP) level, apoptotic and antiapoptotic gene expression, oxidative stress-induced DNA damage, and DNA repair genes. PtNPs and DOX significantly inhibited U2OS viability and proliferation in a dose-dependent manner, increasing lactate dehydrogenase leakage, ROS generation, and malondialdehyde, nitric oxide, and carbonylated protein levels. Mitochondrial dysfunction was confirmed by reduced MMP, decreased ATP levels, and upregulated apoptotic/downregulated antiapoptotic gene expression. Oxidative stress was a major cause of cytotoxicity and genotoxicity, confirmed by decreased levels of various antioxidants. Furthermore, PtNPs and DOX increased 8-oxo-dG and 8-oxo-G levels and induced DNA damage and repair gene expression. Combination of cisplatin and DOX potentially induce apoptosis comparable to PtNPs and DOX. To the best of our knowledge, this is the first report to describe the combined effects of PtNPs and DOX in OS.
六、结语
盐酸多柔比星脂质体的成功,证明了“经典药物+先进递送技术”在现代制药中的巨大潜力。
面对脂质体药物全球化生产的趋势,中新康明以高标准工艺开发、稳定中试放大与公斤级GMP生产能力,为药企提供可靠的脂质体CDMO合作平台,助力更多创新药物实现临床价值。
 返回
返回