随着 mRNA 疫苗在疫情中的成功应用,以脂质纳米颗粒(LNP)为核心技术的 mRNA 递送系统正迎来前所未有的发展机遇。然而,最新发表于《Journal of Controlled Release》的研究揭示:LNP 的物理化学性质(如粒径、PDI、包封率)虽能反映工艺质量,却无法准确预测其体内外效力。这为 mRNA-LNP 的理性设计与高效转化提出了新的挑战,也指明了新的研发方向。
一、mRNA-LNP 研发新趋势:从“性状一致”到“效力驱动”
传统上,LNP 的开发高度关注其关键质量属性(CQAs),如粒径小于 100 nm、低分散度、高包封率等。然而,英国斯特拉斯克莱德大学与以色列理工学院等机构的联合研究表明,即使 CQAs 高度相似,不同脂质组合制备的 LNP 在体内外表达效率仍存在巨大差异。
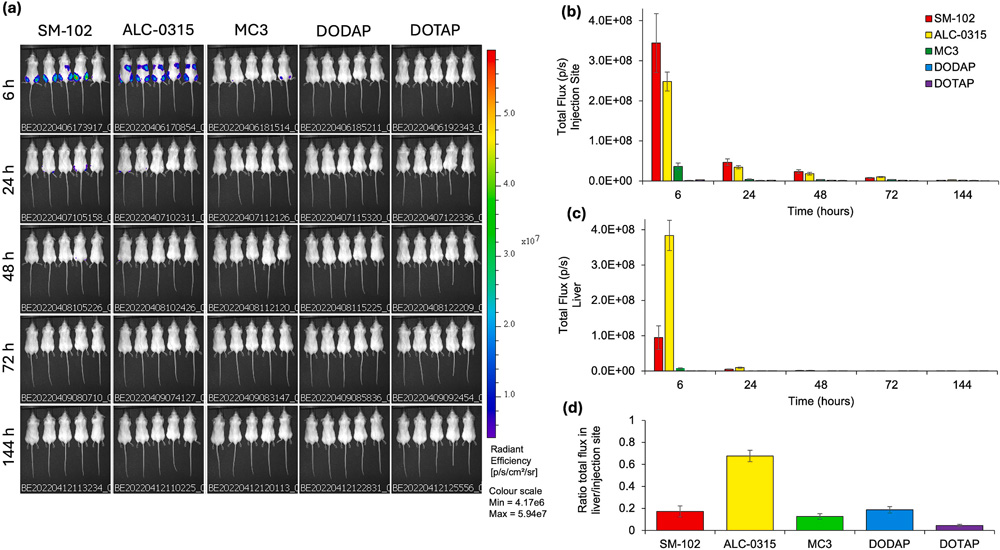
可离子化脂质是效力的关键:研究比较了 SM-102、ALC-0315、MC3、DODAP 和 DOTAP 等常用脂质。在体外(HEK293 细胞)中,SM-102 表现最优;而在小鼠体内,ALC-0315 与 SM-102 效力相当,且显著优于其他脂质。这提示我们:pKa 值、分子几何形状(尤其是支链尾部带来的锥形结构)是影响内体逃逸与表达效率的核心因素,而单纯的 pKa 匹配并不足以预测体内表现。
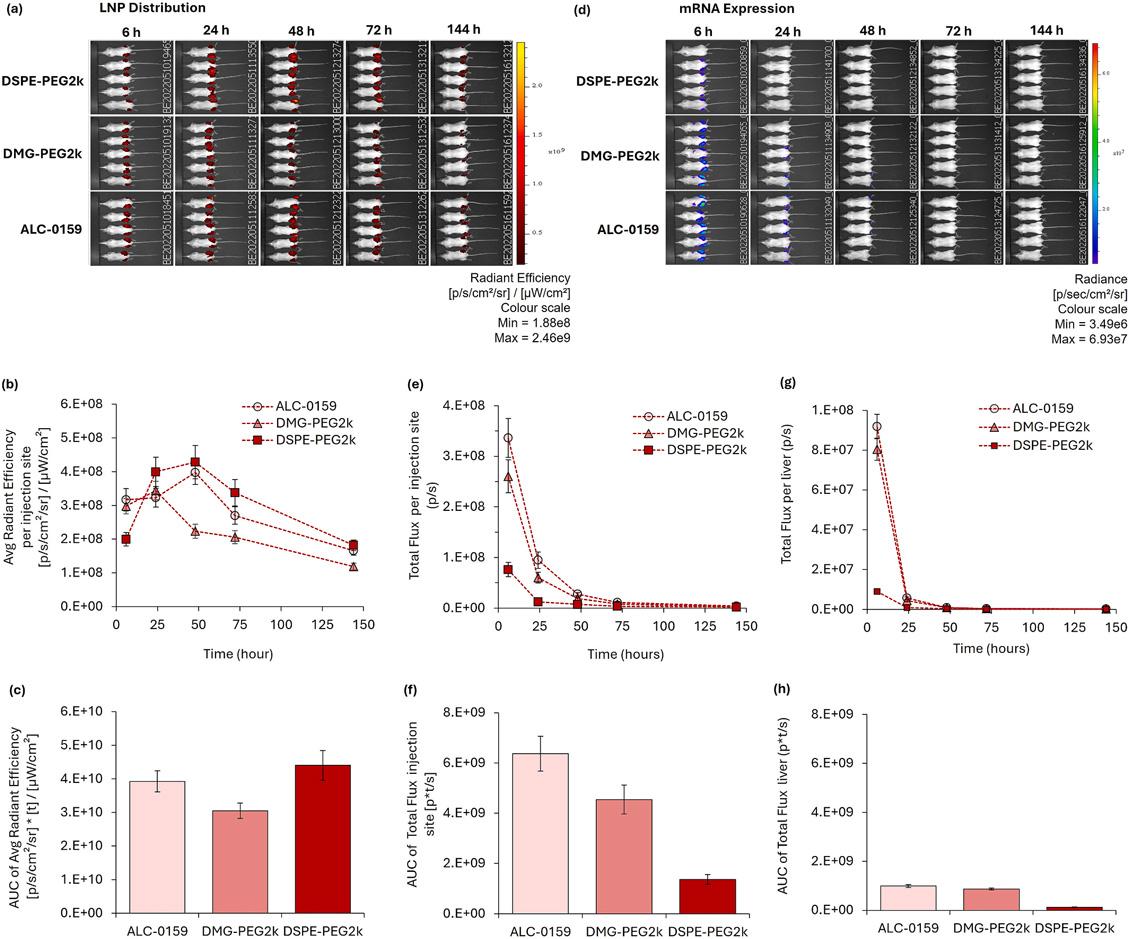
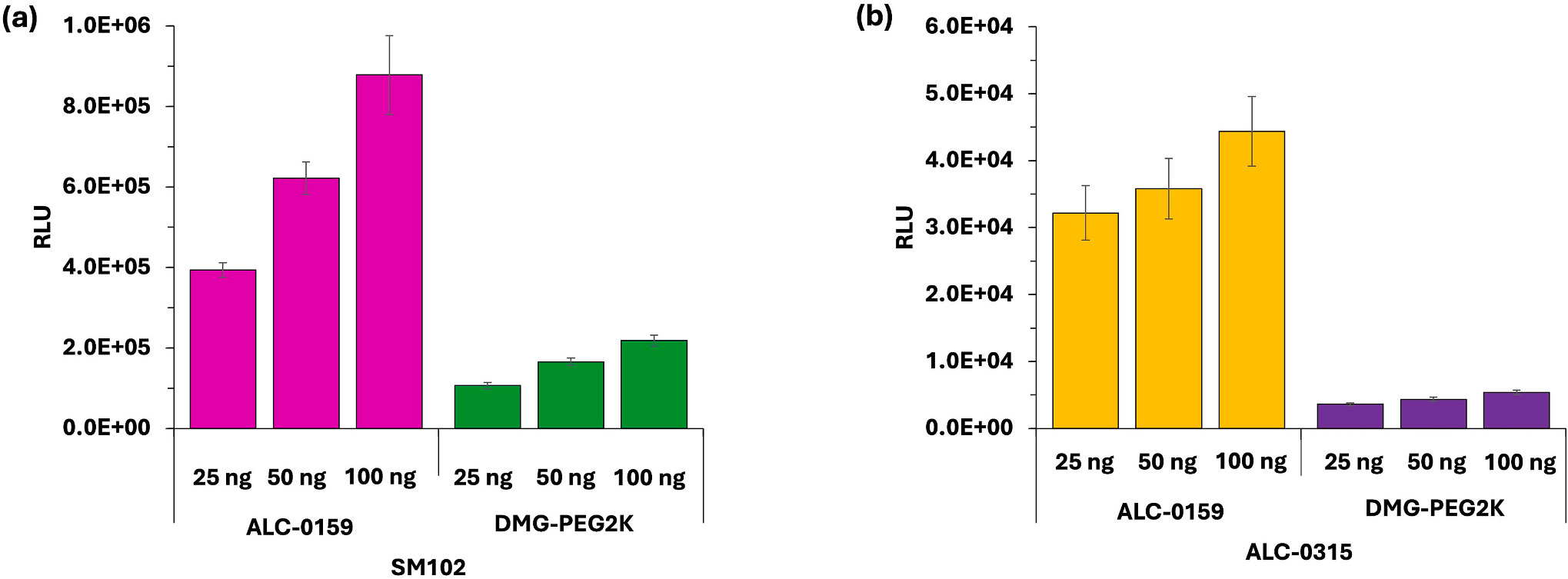
PEG 脂质选择影响显著:研究表明,PEG 脂质的疏水尾链长度直接影响其在体内的解离速率与蛋白表达。长链 PEG(如 DSPE-PEG2k,C18 尾)会显著降低 mRNA 表达,而短链 PEG(如 ALC-0159、DMG-PEG2k,C14 尾)更有利于递送效率。此外,PEG 脂质与可离子化脂质之间存在协同效应,ALC-0315 与 ALC-0159 的组合展现出最高的体内蛋白表达。
体外-体内相关性薄弱:研究再次印证,基于单一细胞系(如 HEK293)的体外筛选难以预测体内效力,凸显了在研发早期引入体内评价与多模型验证的必要性。
这些发现为行业指明了下一阶段的研发重点:应从“工艺导向”转向“效力与机制导向”,通过系统性的脂质筛选、组合优化与体内外综合评价,实现 LNP 的精准设计。
二、中新康明:您的一站式非GMP级 mRNA-LNP 研发合作伙伴
面对 mRNA-LNP 研发中的复杂挑战,中新康明凭借在脂质纳米递送系统领域多年的技术积累与平台化服务能力,为全球科研机构、生物技术企业提供 从原料到数据、从设计到分析的完整 CDMO 解决方案,助力客户加速从概念到临床前候选物的转化。
1. 高质量非GMP级原料供应与定制合成
我们提供包括:
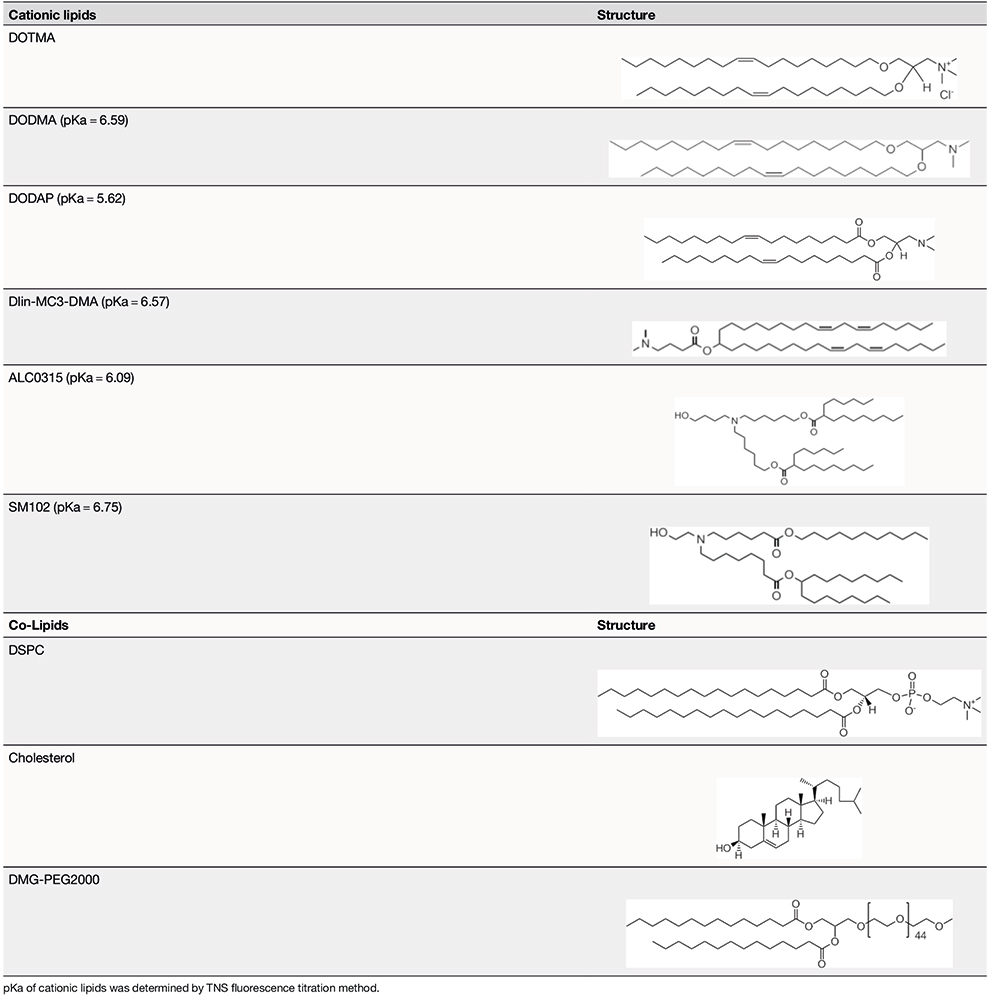
可离子化脂质:SM-102、ALC-0315、DLin-MC3-DMA(MC3)、DODAP、DOTAP 等常用及新型类似物;
PEG 脂质:ALC-0159、DMG-PEG2000、DSPE-PEG2000 等,支持不同链长与功能化修饰;
辅助脂质:DSPC、DOPE、胆固醇及其衍生物;
定制合成服务:可根据客户需求,设计并合成具有特定 pKa、支链结构或可降解链接的新型脂质分子。
所有原料均提供完整的分析证书(COA),包括结构确证、纯度检测、理化性质等数据,确保研发的可靠性与一致性。
2. 全面的 LNP 制备与表征服务
我们采用微流控(如 staggered herringbone mixer)、薄膜水化等先进工艺,为客户提供:
处方筛选与优化:基于设计-实验(DoE)方法,系统研究脂质比例、N/P 比、缓冲体系等对 LNP 性质的影响;
LNP 制备与下游处理:包括乙醇去除、透析、浓缩、无菌过滤等;
全方位表征分析:
粒径、PDI、zeta 电位(DLS)
mRNA 包封率与载量(RiboGreen 法)
结构形态(TEM、cryo-EM)
稳定性研究(加速、长期)
体外释放与降解动力学
3. 体内外功能评价平台
为弥补“体外-体内鸿沟”,我们建立多层次效力与安全性评价体系:
体外评价:
细胞毒性(Alamar Blue、MTT)
转染效率(报告基因如 Luciferase、GFP)
细胞摄取与内体逃逸(共聚焦、流式)
免疫激活效应(细胞因子检测)
体内评价:
药代动力学与组织分布(活体成像,如 DIR/荧光标记)
靶器官表达效率(生物发光/荧光定量)
初步安全性评估(临床病理、组织学)
三、技术优势:为什么选择中新康明?
脂质化学与处方设计的深度整合
我们不仅提供脂质原料,更具备深厚的脂质结构与功能关系(SAR)研究能力,可帮助客户理解不同脂质组合对 LNP 形成、稳定性、细胞内递送与表达的影响,实现理性处方设计。
高通量筛选与平台化能力
依托自动化微流控平台与高通量分析设备,我们可快速完成数十至上百个处方的并行制备与表征,大幅缩短研发周期。
数据驱动的开发策略
我们强调数据的系统性与可追溯性,为客户提供完整的实验报告、原始数据与可视化分析,支持专利申请、IND 申报与科学发表。
灵活的合作模式
支持从“原料+工艺”委托开发到“设计-制备-评价”全流程外包,可根据客户项目阶段灵活调整服务内容。
四、案例分享:助力创新 LNP 递送系统开发
案例背景:一家专注于肿瘤新抗原 mRNA 疫苗的初创企业,需开发一种能够高效递送至抗原呈递细胞(APCs)并激发强效 T 细胞应答的 LNP 载体。
中新康明服务内容:
基于客户目标(靶向 APC、增强免疫原性),我们推荐并合成了系列具有不同 pKa、支链结构与可降解链接的新型可离子化脂质;
采用 DoE 方法筛选了脂质组成、PEG 类型与比例,制备了 48 种 LNP 处方;
系统评价了各处方在树突状细胞系的转染效率、细胞因子分泌与细胞毒性;
最终筛选出 3 个候选处方,在小鼠模型中验证其淋巴结靶向能力与抗原特异性 T 细胞激活效果。
项目成果:在 4 个月内完成从设计到体内概念验证,客户获得一套完整的处方-性能数据集,并成功推进至临床前开发阶段。相关数据支持了其首轮融资与专利布局。
五、中新康明 CDMO 综合服务:从分子到数据的全链条支持
中新康明的使命是成为 mRNA-LNP 领域创新研究的“加速器”与“赋能者”。我们不仅仅是一个供应商或服务商,更是您研发团队的外部延伸。我们的综合服务涵盖:
前端咨询与方案设计:基于您的递送目标(疫苗、治疗、基因编辑等),提供脂质选择、处方策略与评价路径的科学建议;
原料-制备-表征一体化:确保从分子结构到纳米颗粒的全程质量控制与数据连贯;
功能评价与机制探索:通过多层次生物学实验,帮助您理解 LNP 的细胞内命运与效力机制;
报告与知识产权支持:提供符合期刊发表与监管要求的详细实验报告、图表与数据包,协助您进行知识产权保护与申报资料准备。
在 mRNA 疗法蓬勃发展的今天,递送系统仍是其临床转化的核心瓶颈。中新康明愿以专业的技术平台、丰富的项目经验与灵活的协作模式,与您共同攻克 LNP 研发中的挑战,助力您的创新想法早日成为现实。
 返回
返回