一、综述
SM-102(CAS:2089251-47-6)是一种可电离阳离子脂质,分子式为C₄₄H₈₇NO₅,分子量710.2。其氮原子在酸性条件下可质子化形成阳离子,能与带负电荷的核酸结合形成稳定复合物,是mRNA疫苗及基因治疗药物递送系统的核心辅料,广泛应用于脂质纳米颗粒(LNP)制备。
二、中新康明SM-102全链条服务体系
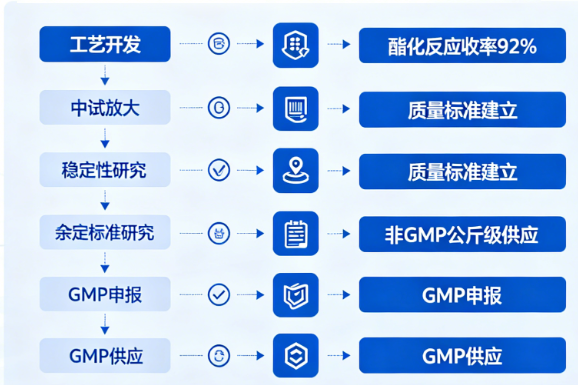
中新康明依托多年功能脂质合成、工艺优化及放大生产技术积累,为客户提供SM-102从工艺开发到非GMP公斤级供应的全链条服务,覆盖工艺开发、中试放大、杂质研究、稳定性研究、质量标准建立、非GMP公斤级供应、GMP申报及GMP供应等核心环节。各环节均建立标准化流程与严格质量管控,可有效降低客户研发及生产风险、加速项目推进,目前已实现酯化反应收率92%、杂质控制在3种以内,达成99.2%纯度的公斤级生产水平。
三、工艺开发
核心目标:聚焦SM-102合成工艺的高效性、稳定性及经济性,结合前沿专利技术与自身研发经验,形成可直接对接中试生产的标准化工艺方案,为放大生产奠定基础。
核心工作内容及成果
路线筛选:采用还原胺化等更优反应方式,规避传统卤代烃烷基化反应中季铵盐杂质生成、高温氧化降解等问题,实现室温高效反应,获得无色高纯度产物。
参数优化:通过单因素与正交实验,系统优化原料配比、反应温度、搅拌速率、反应时间、催化剂用量等关键参数,解决收率偏低、副产物过多、产物颜色异常等行业痛点。
后处理优化:整合过滤、萃取、柱层析、重结晶等纯化方式提升产物纯度,同步开展工艺可行性验证,规避中试及工业化放大潜在风险,确保工艺可复制、稳定。
关键指标
| 关键步骤 | 收率目标 | 反应条件 | 产物状态 |
EDCI酯缩合 | ≥85% | 室温 | 无色、高纯度 |
四、中试放大技术
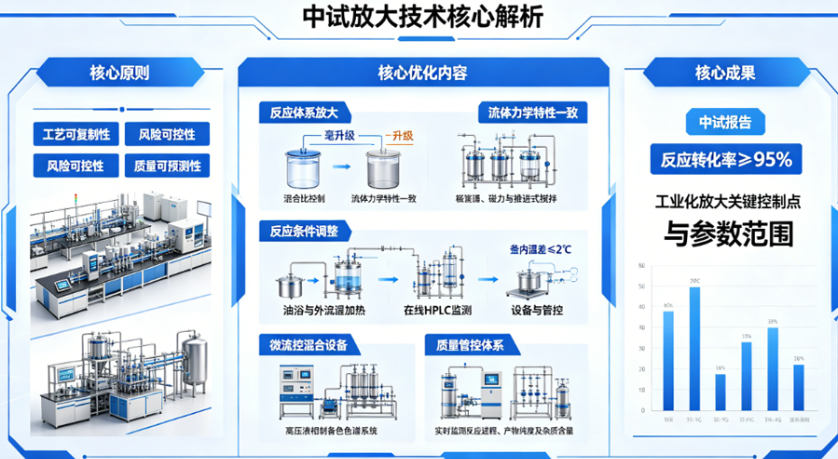
核心原则:遵循“工艺可复制性、风险可控性、质量可预测性”三大原则,以实验室优化工艺为基础,搭建标准化中试生产线,实现SM-102从实验室小试到中试的平稳过渡,解决“放大效应”带来的技术难题。
核心优化内容
反应体系放大:从毫升级提升至升级,严格控制脂质乙醇相与水相缓冲液混合比,保障微混合器内流体力学特性一致,确保产物均一性。
反应条件调整:适配小试与中试设备差异,调整加热方式(油浴→外循环)、搅拌类型(磁力→推进式),控制釜内温差≤2℃,结合在线HPLC监测反应进度。
设备与管控:配备微流控混合设备、高压液相制备色谱系统等核心设备,建立完善中试质量管控体系,实时监测反应进程、产物纯度及杂质含量,留存关键数据。
核心成果:形成中试报告,明确工业化放大关键控制点与参数范围,确保中试产品质量与小试一致,反应转化率≥95%,为工业化生产提供精准数据支撑与技术指导。
五、杂质研究
核心目标:依托先进检测设备,开展SM-102全生命周期杂质研究,覆盖杂质识别、定性、定量及控制全流程,确保产品安全性与纯度达标,契合医药辅料严格质量要求。
核心研究内容
杂质类型分析:系统梳理合成过程中可能产生的原料残留、中间体杂质、反应副产物(如叔胺、季铵盐)、降解杂质(如高温氧化、酯键断裂产物),重点识别关键杂质。
杂质控制策略:针对季铵盐等难分离杂质,从原料配比、反应条件优化(源头)及萃取、成盐分离(纯化过程)双管齐下,减少杂质生成、去除现有杂质。
检测方法验证:建立精准的杂质定量检测方法,通过方法学验证,确保检测准确性、灵敏性与重现性,严格控制杂质含量。
核心成果:形成完整杂质研究报告,明确杂质控制限度,确保产品纯度符合非GMP级≥98%要求,为质量标准建立及工艺优化提供科学依据。
六、稳定性研究
核心目标:按照国际药典及各国药品监管机构要求,开展SM-102系统性稳定性研究,全面评估产品在不同环境下的化学、物理及微生物稳定性,明确储存条件、有效期及质量变化规律,为产品生产、储存、运输及使用提供科学指导。
研究内容与条件
| 研究维度 | 监测重点 | 考察条件 | 关键结论 |
化学稳定性 | 主成分含量、降解杂质生成 | 温度(-20℃、25℃、40℃)、pH、氧化应激 | 低温可维持稳定,常温/高温易降解 |
物理稳定性 | 溶解性、粒径分布、凝聚性 | 同上述考察条件 | 低温下物理性状稳定 |
微生物稳定性 | 微生物污染风险 | 不同温湿度条件 | 规范储存可规避污染风险 |
核心试验:开展加速稳定性试验(40℃、75%湿度)、长期稳定性试验(推荐储存条件)及应力试验(极端条件),采用多种检测方法周期性监测。
核心成果:确定最佳储存条件(-20℃密封储存)、有效期及运输要求,形成完整稳定性研究报告,为质量标准设定提供依据。
七、质量标准建立
核心原则:遵循“全面、针对性、可行、可控”原则,结合杂质研究、稳定性研究及工艺特点,参考化学药物质量标准建立规范,构建科学、合理、可落地的质量标准体系,确保产品质量可控、批间一致,对接后续GMP申报标准。
质量标准核心内容
基础信息:产品通用名、英文名、化学结构式、分子式、分子量、性状、理化性质等。
鉴别项:明确产品专属鉴别方法,保障产品特异性。
检查项:涵盖纯度检查(有关物质、杂质限度)、一般杂质检查(氯化物、硫酸盐等)、残留溶剂检查、干燥失重/水分测定,增设粒径分布、凝聚性等专项检查。
含量测定:建立精准检测方法,确保非GMP级产品纯度≥98%。
其他:明确贮藏条件、有效期等,规范质量控制要求。
核心保障:所有检测方法均经过系统方法学验证,可根据客户需求及应用场景针对性调整,形成完整质量标准文件,为生产检测、质量验收、市场准入提供依据。

八、非GMP公斤级供应
核心目标:依托成熟中试放大工艺及标准化生产流程,实现SM-102非GMP级公斤级规模化供应,满足客户实验室研发、小批量生产及临床前研究需求,打破行业供应瓶颈,保障质量稳定、供应及时、性价比优越。
核心供应优势
| 研究维度 | 监测重点 | 考察条件 | 关键结论 |
化学稳定性 | 主成分含量、降解杂质生成 | 温度(-20℃、25℃、40℃)、pH、氧化应激 | 低温可维持稳定,常温/高温易降解 |
物理稳定性 | 溶解性、粒径分布、凝聚性 | 同上述考察条件 | 低温下物理性状稳定 |
微生物稳定性 | 微生物污染风险 | 不同温湿度条件 | 规范储存可规避污染风险 |
九、GMP申报
核心服务:依托专业GMP申报团队及丰富行业经验,提供SM-102 GMP认证申报全流程协助服务,助力客户顺利通过GMP认证,推动产品产业化、商业化转型(目前GMP级暂不供应,可联合开发)。
全流程服务内容
前期准备:梳理申报要求,结合产品相关研究数据,制定个性化申报方案,明确重点及时间节点。
资料撰写:协助撰写工艺规程、质量标准、各类研究报告等完整申报资料,确保规范、准确,契合国内外申报要求。
申报跟进:提交申报后,跟进进度,响应监管部门问询,补充相关资料、解答疑问。
现场审核配合:梳理现场重点,开展模拟审核,排查问题并指导整改,全力配合监管部门现场审核,确保通过认证。
核心价值:为客户实现SM-102 GMP级规模化生产及市场准入提供全方位支持,助力抢占市场先机。
十、中新康明产品服务范围
脂质体及LNP辅料磷脂:DPPC、DSPE、DOPE、DOTAP、SM-102、新脂质结构等;
聚乙二醇修饰及衍生物:DSPE-PEG2000、MPEG-NH2、COOH-PEG-COOH、新偶联结构等;
ADC PEG Linkers:N3-PEG4-NH2、N3-PEG3-COOH等;
荧光染料:Fluorescein、Rhodamine B、Cy3、Cy5、Cy7、ICG等;
APIs小分子药物及医药中间体:分子砌块、先导化合物、中间体、APIs、前药等。
十一、相关应用案例
某生物制药企业mRNA疫苗研发项目,需SM-102作为LNP递送系统核心辅料,用于临床前研究,要求纯度≥98%、供应规模5kg、交付周期60个工作日。
中新康明快速启动工艺匹配与优化,调整参数重点控制季铵盐等难分离杂质,通过重结晶与柱层析纯化确保纯度达标;高效推进中试生产,严格把控过程质量,按时完成5kg非GMP级SM-102供应,并提供完整COA报告及相关研究资料。
该批次产品成功应用于LNP制备,包封效率达95%以上、稳定性良好,助力客户顺利完成临床前动物实验,项目推进效率较预期提升20%,获得客户高度认可。

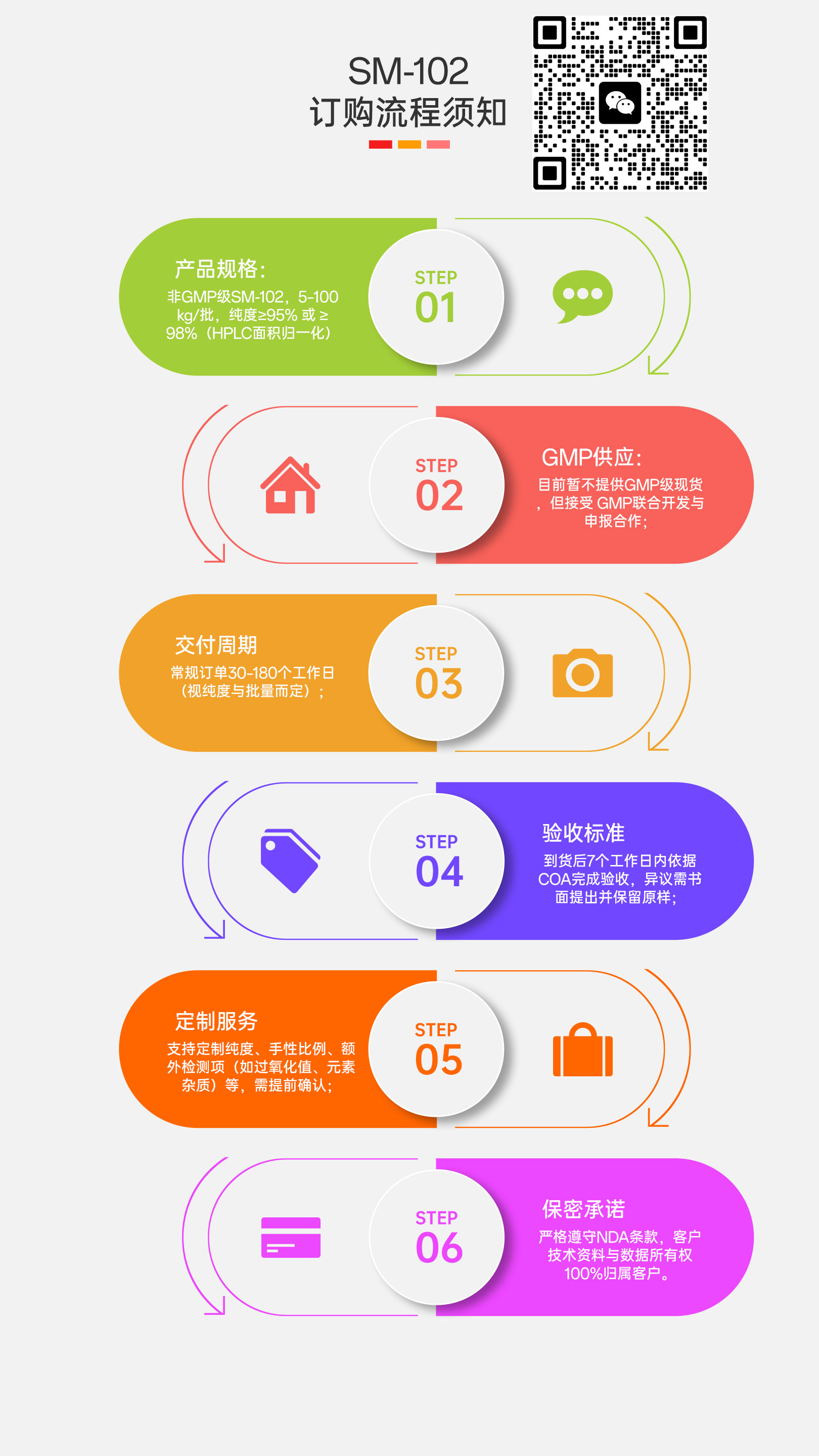
十二、订购流程及核心须知
产品等级:
非GMP级:5–100 kg/批,纯度≥95% 或 ≥98%(HPLC)
GMP级:接受联合开发,支持DMF/ASMF备案,最小批量5 kg
交付周期:
非GMP:30–90个工作日
GMP:90–180个工作日(含方法验证与审计准备)
包装与运输:
1 kg / 5 kg 铝箔复合袋(充氮密封,带干燥剂)
20 kg 不锈钢桶(PTFE内衬,–20°C预冷)
全程–20°C冷链运输,附COA、SDS、过氧化值报告、手性分析图谱
验收条款:到货7日内依据COA验收,异议需保留原包装并书面提出
定制选项:
指定过氧化值上限(如≤3 meq/kg)
增加元素杂质(ICP-MS)、基因毒性杂质筛查
提供稳定性研究数据(加速/长期)
保密承诺:项目启动前签署NDA,所有数据、工艺、成果归属客户
中新康明——不止是脂质供应商,更是您值得信赖的核酸药物CDMO合作伙伴。
从SM-102到LNP成品,我们为您的创新疗法提供端到端、合规、可靠的解决方案。
欢迎垂询 SM-102、ALC-0315、MC3、DOTAP、LP01 等LNP核心脂质的CDMO开发、GMP生产与全球供应链服务。
 返回
返回