随着骨科植入物、再生医学与高端医疗器械市场快速增长,具备抗菌能力、生物相容性与成骨促进的新型支架材料,正成为行业关注的重点。基于对临床需求和材料创新趋势的深度洞察,中新康明成功构建了聚羟基脂肪酸酯(polyhydroxyalkanoate,PHA)功能化微球平台(p-PHA),并通过系统验证证实其在抗菌、促成骨分化与生物安全性方面具备优异性能。
依托成熟的材料制备工艺与CDMO服务体系,中新康明不仅能够研发高性能p-PHA微球,更可提供大包装材料供应、质量检测、活性分子负载、处方工艺优化及临床前支持等全流程服务,帮助企业与科研机构快速推进项目落地。

01 | 新一代骨组织工程材料:p-PHA微球的商业化价值
PHA是一种来源稳定、可降解性优异的天然聚合物,近年来在骨修复、再生医学、医用注射填充物等领域需求持续扩大。在此基础上,中新康明构建的p-PHA微球平台具有以下显著优势,为企业加速产品研发与商业化提供了更多可能:
▶高生物相容性,为骨修复提供安全载体
p-PHA微球在细胞黏附、增殖与长期接触实验中表现出卓越生物安全性,适用于药械组合(combinationproduct)、骨修复支架、骨填充物及可注射材料开发。
▶功能化能力强,可组合BMP-2与抗菌肽
通过优化微球结构设计,材料可同时负载BMP-2、生物活性肽、抗菌肽(如hBD-3)等,实现单一材料的多重功效,在骨修复产品端体现更高的差异化价值。
▶支持可控释放,提高实际应用效果
公司通过调控微球孔结构、聚合物组成与蛋白保护技术,成功实现BMP-2的缓释与活性保持,在促成骨分化实验中效果显著。
这些产品性能为企业快速构建具有竞争力的骨修复解决方案提供了产业基础,也使p-PHA微球成为新一代支架材料的潜力选择。
02 | 中新康明的制备优势:可提供大包装与稳定供货体系
在产业端,材料稳定供应能力是推动创新产品落地的核心。依托内部工程化设备与规模化制备工艺,中新康明可为客户提供:
▶大包装供应能力:适配从科研到产业全过程
标准规格:10g、50g、100g
中试级:500g、1kg
商业化级:多公斤级稳定放大生产
无论您是处于早期探索,还是准备申报与放大,我们都可提供符合检测标准的高一致性p-PHA微球材料。
▶多粒径、可定制结构与功能化方案
粒径范围:5μm–200μm
支持空心、多孔、核壳结构调控
支持药物负载、蛋白固定化、双因子共载
支持根据不同植入路径调控降解速率
公司可基于客户应用场景(如可注射微球、骨填充物、复合支架)提供针对性的结构化设计。
03 | 全面的表征与验证服务:直接支持研发、专利与注册申报
为了帮助合作伙伴快速推进研发,中新康明可提供覆盖材料科学、生物学评价与生物活性验证的完整检测体系,输出标准化数据包,适用于项目评估、科研发表与注册前准备。
| 中新康明表征与验证服务 | |||
| 材料性质表征 | 粒径/PDI | SEM形貌 | 分子量/端基/纯度 |
| 热性能(DSC、TGA) | 力学强度与水解降解曲线 | 载药与释放相关检测 | 包封率、载药量 |
| 蛋白活性保持(SDS-PAGE、ELISA) | 体外释放曲线 | 多模型动力学拟合 | 生物学性能验证 |
| 细胞毒性与增殖(CCK-8、Live/Dead) | hBMSCs黏附、铺展、形态成像 | ALP活性与ARS钙化水平 | 成骨基因表达(RT-qPCR) |
| 抗菌性能(抗菌圈、MIC、MBC) | |||
所有数据均可形成标准化、可溯源的检测报告,用于内部研发、合作沟通以及备案用途。
04 | 从配方到生产:中新康明提供专业的p-PHA微球CDMO服务
面对企业不断增长的产品上市和临床评估需求,中新康明构建了完整的制剂CDMO服务链条,帮助客户从概念验证(PoC)到稳定生产,实现研发—中试—申报的一站式落地。
▶配方与工艺开发
PHA微球配方筛选
多因子DOE优化
稳定性提升策略
▶工艺放大与规模化生产
乳化、微流控、喷雾干燥等多种可选路径
工艺放大验证(CPP、CQA体系建立)
设备适配与连续性优化
▶质量体系与申报支持
COA、DMF文件准备
质量研究报告
申报所需原始记录文件
合作CRO的体内评价资源对接
无论是医用材料企业、药械组合产品开发者,还是高校与科研团队,我们都可以提供可直接用于临床前开发的系统化服务。
参考文献:“功能化聚羟基脂肪酸酯微球的制备及其抗菌、促成骨分化功能评价”
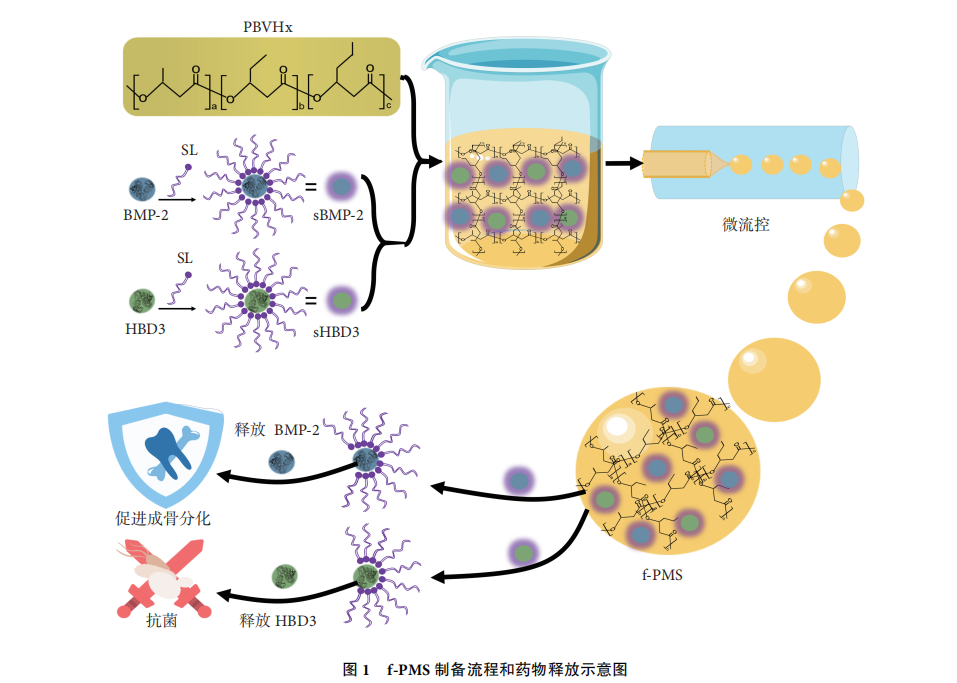
文献节选: 构建负载 BMP-2 和人 β 防御素 3(human β-defensin 3,HBD3)的聚羟基脂肪酸酯
(polyhydroxyalkanoate,PHA)微球,并评估其抗菌性、生物相容性以及促成骨分化效果,旨在为骨组织工程提供一种新的支架材料。
方法:采用大豆磷脂(soybean lecithin,SL)介导的生长因子修饰技术制备 SL-BMP-2 和 SL-HBD3,再利用微流控技术制备含有 BMP-2 及 HBD3 的功能化 PHA 微球(functional microsphere,f-PMS),同法制备单纯 PHA 微球(pure microsphere,p-PMS)作为对照。然后,通过扫描电镜观察两种微球形貌、检测吸水率,并利用 ELISA 试剂盒检测 f-PMS 中 BMP-2 和 HBD3 释放规律;采用活/死细菌染色观测两种微球在金黄色葡萄球菌以及大肠杆菌悬液中的抗菌效果;采用与人 BMSCs 共培养,通过 Transwell 和细胞计数试剂盒 8 检测微球生物相容性,以及Ⅰ型胶原(collagen type Ⅰ,COL-1)免疫荧光染色和 ALP 浓度测定来判定微球促成骨分化作用
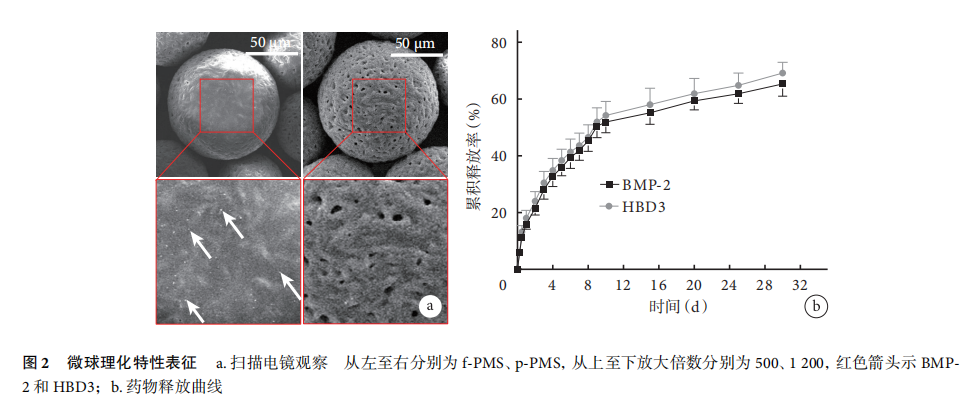
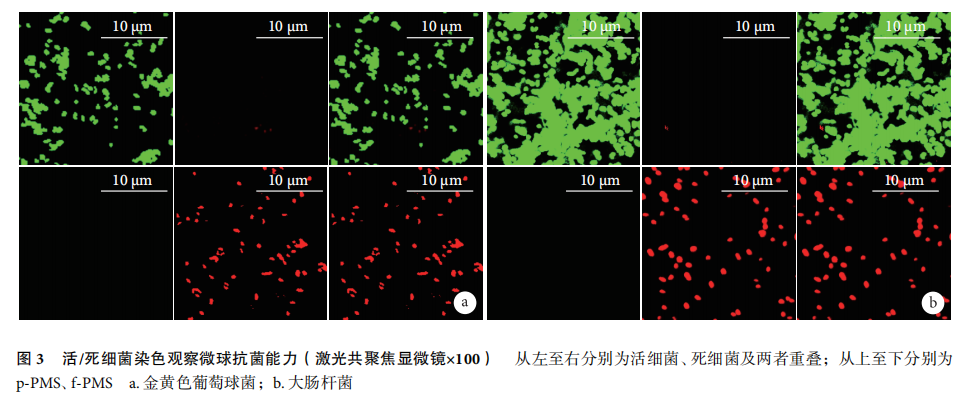
结果:实验成功构建 f-PMS 及 p-PMS 两种微球。扫描电镜观察示 p-PMS 表面粗糙,分布直径 1~3 μm 的孔隙;而f-PMS 表明光滑,且存在白色颗粒状物质;两组吸水率差异无统计学意义(P>0.05);f-PMS 中 BMP-2 和 HBD3 释放曲线基本一致,均呈现早期突释、后期缓释规律。f-PMS 能抑制金黄色葡萄球菌及大肠杆菌生长,且抗菌性高于 p-PMS,差异有统计学意义(P<0.05);但两种微球生物相容性差异无统计学意义(P>0.05)。免疫荧光染色示 fPMS 成骨特异性蛋白 COL-1 荧光强度高于 p-PMS,ALP 浓度高于 p-PMS,差异均有统计学意义(P<0.05)。
结论:p-PHA 具有良好的抗菌能力和生物相容性,并且能促进 hBMSCs 成骨分化,有望作为骨组织工程支架材料。
05 | 赋能骨修复创新:p-PHA微球的未来应用版图
在骨科植入、骨缺损修复、药物缓释载体和个体化再生医学领域,p-PHA微球均具备广阔的发展潜力:
可注射骨修复微球
BMP-2缓释载体
抗菌活性支架
复合支架(与TCP、HA、胶原等共混)
组织再生产品中的组合单元
药械组合类产品开发
凭借材料基础性能与可负载能力的双重优势,p-PHA微球为企业布局高性能、差异化骨修复产品提供了坚实的平台。
结语:中新康明,用可产业化材料技术赋能产品落地
从材料研发、结构设计、活性分子负载,到中试放大、检测验证、工艺开发与CDMO服务,中新康明已具备面向商业化落地的全链条能力。p-PHA微球平台的推出,将为企业在骨组织工程、再生医学和创新材料领域提供更高效、更经济、更可执行的解决方案。
 返回
返回